Perbedaan Antara Sintesis Hidrolisis dan Dehidrasi
Perbedaan Antara Sintesis Hidrolisis dan Dehidrasi
Biosintesis sangat penting dalam semua organisme hidup - ini adalah integrasi kehidupan. Ini adalah proses organik, yang melibatkan senyawa sederhana untuk dimodifikasi, digabungkan atau diubah menjadi senyawa lain untuk membentuk makromolekul. Ada dua proses yang memainkan peran penting dalam biosintesis. Ini adalah Hidrolisis dan Sintesis Dehidrasi.
Hidrolisis dan Dehidrasi Sintesis keduanya berhubungan dengan air dan molekul lainnya, namun dengan cara yang sangat berbeda. Keduanya memiliki reaksi terbalik dalam hubungan satu sama lain dan sebaliknya. Dalam biologi, proses ini melibatkan pembentukan Polimer, ini adalah molekul yang dihubungkan secara kovalen. Ini terbentuk saat air dikeluarkan dari persamaan kimia, kemudian molekul monomer (molekul kecil) digabungkan. Untuk memecahkan ikatan, air harus ditambahkan ke persamaan. Untuk lebih memahami hal ini, informasi rinci mengenai perbedaan antara sintesis hidrolisis dan dehidrasi dibahas di bawah ini.
Hidrolisis
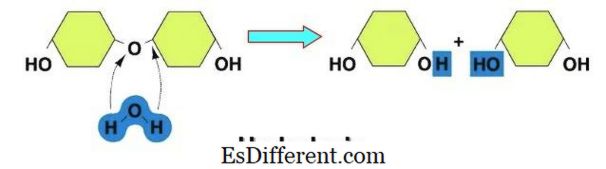
Hidrolisis berarti memisahkan dengan penggunaan air. Itu berasal dari kata Yunani "hydro" yang berarti air, dan "lisis" yang berarti perpisahan. Ketika air ditambahkan ke molekul, ia menghancurkan ikatan H2O menjadi H dan OH yang membentuk molekul terpisah.
Dalam Kimia, Hidrolisis adalah reaksi kimia dengan air, dimana makromolekul dipisahkan menjadi molekul yang lebih kecil. Di sisi lain, dalam Biologi, proses ini melibatkan air untuk memecah polimer menjadi monomer. Intinya adalah Hidrolisis terjadi ketika air ditambahkan ke persamaan untuk memecahnya atau memisahkannya.
Dalam tubuh kita, Hidrolisis adalah proses utama untuk melepaskan energi. Saat kita makan makanan, dicerna atau dipecah menjadi zat sehingga tubuh bisa menyerapnya dan mengubahnya menjadi energi. Makanan, molekul kompleks dipecah menjadi molekul sederhana. Ketika energi dibutuhkan untuk biosintesis, ATP dihidrolisis dan energi yang tersimpan dilepaskan untuk pemanfaatannya.
Dehidrasi Sintesis

Dehidrasi berarti membuang air, dan sintesis berarti membangun atau menciptakan sesuatu. Oleh karena itu, Dehidrasi Sintesis didefinisikan sebagai mengambil air untuk membangun sesuatu. Proses ini terjadi dengan mengeluarkan satu molekul -OH (gugus hidroksil) dan satu molekul -H membentuk H2O atau air. Hal ini menyebabkan kovalen bergabung dengan dua monomer (molekul kecil) untuk membentuk polimer (molekul yang lebih besar). Sintesis Dehidrasi menggunakan kondensasi dalam proses dan bila ini berlanjut untuk jangka waktu yang lama, rantai panjang dan kompleks terbentuk, seperti yang ada di polisakarida. Hal ini juga bertanggung jawab untuk menyimpan kelebihan molekul glukosa sebanyak polisakarida yang lebih besar seperti pati dan glikogen.
Contoh Sintesis Hidrolisis dan Dehidrasi
Hidrolisis dan Dehidrasi Sintesis bekerja dengan cara yang sama dengan protein, karbohidrat, asam nukleat dan lipid. Seperti disebutkan sebelumnya, dalam proses Hidrolisis - ketika air ditambahkan, ia memisahkan ikatan antara oksigen dan hidrogen dan reformasi menjadi dua hidroksil yang terpisah. Sebaliknya, dalam proses Dehidrasi Sintesis Anda memiliki hidroksil di setiap sisi, jadi jika oksigen dan dua hidrogen dikeluarkan dan mengikat sisa oksigen ke hidrogen yang tersisa untuk membentuk polimer.
Karbohidrat


