Perbedaan antara Oktet dan Duplet | Octet vs Duplet
Perbedaan Kunci - Oktet vs Duplet
Ada atom dan senyawa aktif secara kimia dan aktif yang ada di alam. Karakteristik ini terutama bergantung pada jumlah elektron yang ada di kerang terluar atom. Atom yang memiliki kerang yang tidak lengkap dapat menjadi aktif untuk melengkapi konfigurasi elektron mereka agar menjadi stabil. Atom yang tidak aktif memiliki konfigurasi elektron yang lengkap; Dengan demikian, atom-atom ini tidak bereaksi dengan atom lain kecuali dalam kondisi khusus. Gas mulia selalu tidak aktif. Oleh karena itu, mereka dikenal sebagai gas inert. Gas inert berada di kolom kedelapan dalam tabel periodik. Elemen lain pada periode yang sama (baris) cenderung mendapatkan konfigurasi elektron gas inert pada akhir periode tersebut, yang merupakan bentuk paling stabil di alam. Atom aktif cenderung melengkapi jumlah elektron sesuai aturan oktet atau aturan dupleter . Perbedaan utama antara oktet dan duplet adalah bahwa oktet adalah atom atau ion yang memiliki maksimum delapan elektron di kulit terluar sementara duplet adalah atom yang memiliki maksimum dua elektron di kulit terluar..
DAFTAR ISI
1. Ikhtisar dan Perbedaan Kunci
2. Apa itu Octet
3. Apa itu Duplet
4. Perbandingan Side by Side - Oktet vs Duplet
5. Ringkasan
Apa itu Octet?
Sebuah oktet adalah atom atau ion yang memiliki delapan elektron di kulit terluar dari atom tersebut. Semua gas mulia kecuali helium memiliki delapan elektron dan bersifat inert. Konfigurasi elektron gas mulia akan selalu berakhir sebagai berikut.
Contoh konfigurasi elektron Neon adalah 1s2 2s 2 2p
6 . Neon adalah gas inert. Elemen-elemen lain yang memiliki tujuh, enam, dan lain-lain. Elektron di orbital terluar cenderung mematuhi peraturan oktet dengan mendapatkan elektron dari luar; beberapa elemen lain yang memiliki satu, dua, dan lain-lain. elektron cenderung kehilangan elektron dan mendapatkan konfigurasi elektron dari gas inert terdekat. Tapi elemen lain di tengah tabel periodik akan membentuk ikatan baru dengan elemen yang memiliki kelebihan elektron untuk berbagi elektron tersebut dan menjadi oktet.
2s
1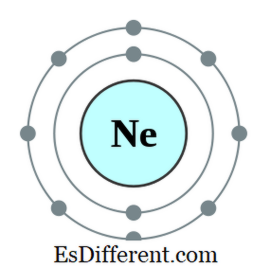
. Dengan melepaskan elektron 2s
1
, itu bisa menjadi dupleter. Dalam kasus ini, He, H - dan Li + adalah dupleter yang dapat eksis sebagai duplet stabil. Semua dupleks memiliki konfigurasi elektron yang diakhiri sebagai berikut. ns 2 Gambar 02: Helium, dupleter Apa perbedaan antara Octet dan Duplet? - diff Article Middle before Table ->
Octet vs Duplet
Octet memiliki delapan elektron di kulit terluar. Duplet memiliki dua elektron di kulit terluar.

Konfigurasi Elektron Umum
Octet memiliki ns
2
np |
|
| 6 | ketik konfigurasi elektron di bagian akhir. |
| Duplet memiliki ns | |
| 2 ketik konfigurasi di bagian akhir. Jumlah Orbitals Oktet mungkin memiliki minimal dua orbital. Dupleting hanya memiliki satu orbital. | Jenis Orbitals Sebuah oktet dapat memiliki semua jenis orbital seperti s, p, d, f, dll. Duplet hanya memiliki orbit orbital. |
| Ringkasan - Octet vs Duplet | |
| Semua elemen cenderung menjadi stabil. Tetapi dengan konfigurasi elektron yang tidak lengkap, atom tidak dapat stabil; Dengan demikian, mereka menjadi sangat reaktif untuk mengisi kerang dengan elektron dengan cara mendapatkan, kehilangan atau berbagi elektron. Atom atau molekul yang mematuhi oktet atau aturan dupleks stabil. Perbedaan utama antara oktet dan dupleter adalah oktet yang memiliki delapan elektron di orbit terluarnya sedangkan duplet memiliki dua elektron di orbitalnya. | Referensi: |
| 1. Nema, P., 2011. Topperlearning. [Online] Tersedia di: // www. topperlearning com / forums / rumah-kerja-bantuan-19 / apa-adalah-oktet-duplet-valensi-dan-ion-kimia-struktur-atom-46317 / balasan [Diakses 29 05 2017]. | |
| 2. Chang, R., 2010. Kimia. 10 ed. New York: McGraw-Hill. | 3. Segera., 2015. Grade stacker. [Online] Tersedia di: // gradestack. com / NTSE-Complete-Course / Chemical-Bonding / Chemical-Activity-of-An / 19176-3853-37737-study-wtw [Diakses 29 05 2017]. |
Gambar Courtesy:
1. "Elektron shell 002 Helium - tidak ada label" Oleh Pumbaa (karya asli oleh Greg Robson) - Diagram shell elektron (versi berlabel yang sesuai) (CC BY-SA 2. 0 uk) via Commons Wikimedia
2. "Elang elektron 010 Neon" Oleh Pumbaa (karya asli oleh Greg Robson) (CC BY-SA 2. 0 uk) melalui Commons Wikimedia




