Perbedaan Antara Sulfur dan Sulfat dan Sulfit | Sulfur vs Sulfat vs Sulfit
Sulfur vs Sulfat vs Sulfit
Bahan kimia memiliki nama yang sangat unik. Sulfat (Sulfat), sulfit (Sulphite), dan belerang (Sulfur) adalah tiga bahan kimia dengan sifat kimia dan fisik yang sangat berbeda. Seorang ahli kimia atau siapa saja yang akrab dengan bahan kimia mungkin tidak memiliki masalah dalam membedakan perbedaan antara ketiga bahan kimia ini, namun bagi seseorang yang tidak dikenal, nama-nama ini terdengar agak sama. Mari kita cari tahu perbedaannya.
-> Apa itu Sulfur?Sulfur adalah unsur non-logam. Simbol kimia Sulfur adalah
S . Hal ini ditemukan di berbagai senyawa dan dalam berbagai bentuk. Jumlah belerang atom adalah 16. Dalam bentuk murni, Sulfur bisa memiliki banyak bentuk fisik. Oleh karena itu, itu disebut elemen allotropik. Yang paling umum adalah warna kuning kristal padat yang sangat rapuh. Elemennya sangat reaktif dan memiliki banyak aplikasi. Ini digunakan dalam bubuk senapan, insektisida dan obat resep dll.
Sulfat adalah Oxy-anion dari Sulfur (Oxy-anion adalah Oksigen yang mengandung ion negatif). Bahkan jika Anda tidak terbiasa dengan Sulfat Anda pasti pernah mendengar tentang asam sulfat. Asam sulfat terdiri dari dua ion H + dan satu ion sulfat. Rumus empiris dari bahan kimia tersebut adalah
SO 4 2- . Ini adalah anion poliatomik. Dalam ion sulfat, atom Sulfur adalah atom pusat dan empat atom oksigen terikat secara kovalen dengan atom Sulfur. Dua atom Oksigen terikat oleh ikatan rangkap dan dua lainnya terikat secara tunggal. Atom Oksigen terikat tunggal awalnya mengandung atom Hidrogen di masing-masingnya. Bila ion sulfat dibuat, mereka melepaskan H + dan membawa muatan negatif. Geometri ion Sulfat adalah tetrahedral dimana atom Oksigen ditempatkan di 4 sudut tetrahedron.

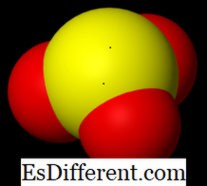
Sulfit adalah satu Oxy-anion of Sulphur yang lain. Ini juga mengandung dua muatan negatif yang mirip dengan ion Sulfat. Perbedaannya terletak pada jumlah atom yang ada dalam ion. Sulfit memiliki tiga atom Oksigen yang berikatan ganda dengan atom Sulfur pusat. Ketika ion H + digabungkan, Sulfit menjadi asam sulfat. Asam ini relatif lebih lemah dibanding asam sulfat. Geometri anion ini adalah trigonal piramidal. Atom Oxygens berada di tiga sisi, dan satu elektron elektron ada di atas. Rumus empiris ion sulfit adalah
SO 3 2- . Kedua anion sulfat ini biasa digunakan dalam pelestarian makanan.
Apa perbedaan antara Sulfur, Sulfat, dan Sulfit? (Sulfur vs Sulfat vs Sulphite)
• Sulfat dan Sulfit adalah Oxy-anion dari Sulfur dan Sulfur adalah suatu unsur.
• Sulfat dan Sulfit membawa muatan negatif, dan Sulfur netral.
• Sulfat memiliki 4 atom Oksigen, dan Sulfit memiliki 3 atom Oksigen. Sulfur adalah unsur murni dimana struktur poliatomiknya hanya mengandung atom Sulfur.
• Sulfat ion memiliki geometri tetrahedral dan Sulfit memiliki geometri piramida trigonal.
• Aplikasi Sulfat, Sulfit, dan Sulfur berbeda. Sulfat dan Sulfit kadang digunakan untuk aplikasi umum seperti pelestarian makanan.




